2016年,我院正式启动申请GCP认定项目,同时成立筹备小组,举全院之力推动项目建设。由GCP办公室负责协调机构各部门、伦理委员会以及专业组的日常事务,按照《中华人民共和国药品管理法》《药物临床试验机构资格认定办法》等有关规定,认真准备资料,组织GCP培训,做好了各项迎检准备工作。
2018年5月25日至26日,国家药品监督管理局专家组对我院药物临床试验的组织管理、药物管理、文件管理、伦理委员会工作以及专业组临床水平和开展试验的能力进行了细致的考核和检查。
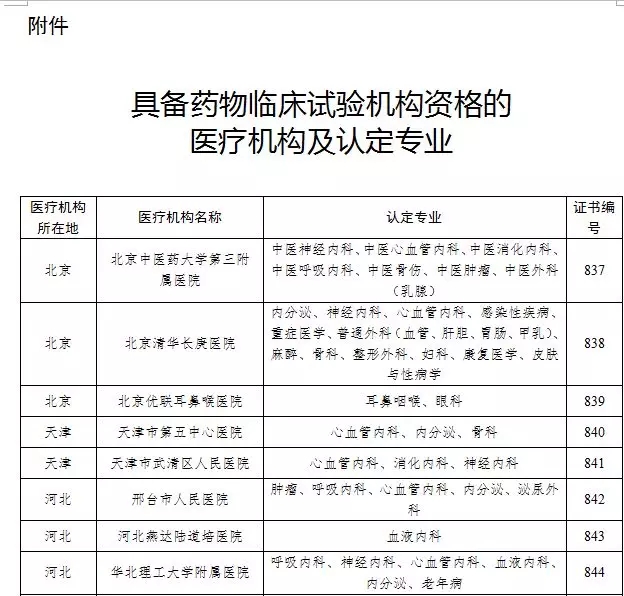
2018年7月18日,国家药品监督管理局在其官方网站上发布了2018年药物临床试验机构资格认定检查公告(第1号),经资料审查和现场检查,认定了沈阳爱尔眼视光医院具有药物临床试验机构资格,取得了GCP证书(编号851号),认定专业为眼科。自此,我院跻身国家药物临床试验资格机构之列,具备了承接药物及医疗器械临床试验的资质。

药物临床试验(GCP)
GCP是在充分保护受试者的基础上,经过伦理委员会审核通过,制定的新药上市前的临床研究阶段,为临床疑难耐药患者提供了新的治疗选择途径。
药物临床试验是指任何在人体(病人或健康志愿者)进行的药物的系统性研究,以证实或发现试验药物的临床、药理和/或其他药效学方面的作用、不良反应和/或吸收、分布、代谢及排泄,目的是确定试验药物的安全性和有效性。所有药物临床试验必须遵循下列三项基本原则,即伦理道德原则、科学性原则、GCP与现行法律法规。
药物临床试验是确证新药有效性和安全性必不可少的步骤,进行药物临床试验需要多种专业技术人员的合作。一个好的临床研究队伍不仅应包括医学、药学、药理学、生物学、生物统计学等专业人员,还应包括非医学专业的但富有经验的文档管理人员。获得药物临床试验资格,是一所医院医疗水平和科研能力的综合体现。因此,是否具备GCP机构资格已被众多医学研究机构、医药高等院校科研团队作为衡量该医疗机构能否合作、承接高质量科研项目的重要标志之一。

此次沈阳爱尔眼视光医院获得GCP资格认定,表明了我院综合能力达到了国家药物临床试验机构要求,使临床医疗水平和临床医学研究能力上升了一个新的台阶,从而推动医院临床医学与科研的发展,带动本地区医疗科研水平的提升,助力医院成为更高水平医院。
作为GCP资格机构,沈阳爱尔眼视光医院将严格按照国家有关规定和标准,进一步完善药物临床试验的管理和质量保证体系,严把临床研究质量关,确保药物临床试验的安全性、有效性和科学评价,从而更好地为群众健康服务。



